Cuales son los elementos mas electronegativos de la tabla periodica
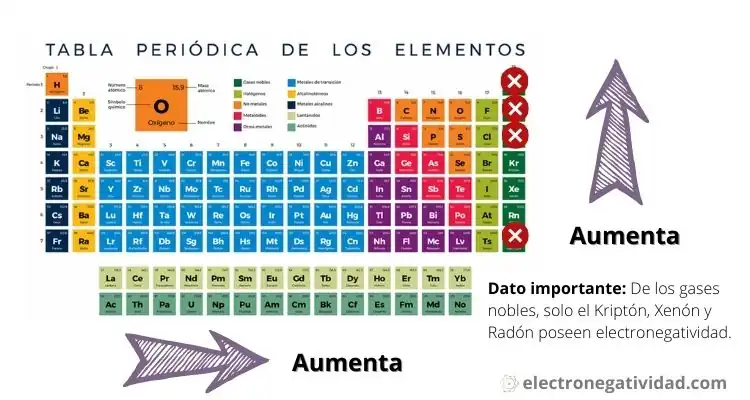
La electronegatividad es una propiedad química que mide la capacidad de un átomo para atraer electrones hacia sí mismo en una molécula. Esta propiedad es fundamental para comprender la polaridad de los enlaces químicos y las reacciones químicas.
- ¿Por qué es importante conocer los elementos más electronegativos?
- ¿Cuáles son los elementos más electronegativos?
- ¿Cómo se mide la electronegatividad?
- ¿Cómo afecta la electronegatividad a los enlaces químicos?
- ¿Qué otros factores influyen en la electronegatividad de los elementos?
- Conclusión y despedida
¿Por qué es importante conocer los elementos más electronegativos?
Conocer los elementos más electronegativos es importante porque nos permite predecir el comportamiento químico de los compuestos. Por ejemplo, si un átomo es muy electronegativo, tendrá una tendencia a atraer electrones hacia sí mismo, lo que puede hacer que el enlace químico sea polar o incluso iónico.
¿Cuáles son los elementos más electronegativos?
Los elementos más electronegativos de la tabla periódica son el flúor (F), el oxígeno (O), el cloro (Cl), el nitrógeno (N), el azufre (S) y el carbono (C). Estos elementos tienen una alta afinidad electrónica y tienden a atraer electrones hacia sí mismos, lo que los convierte en los elementos más electronegativos.
¿Cómo se mide la electronegatividad?
Existen varios métodos para medir la electronegatividad, pero el más común es el método de Pauling. En este método, se asigna un valor de electronegatividad a cada elemento en la tabla periódica, donde el flúor tiene el valor más alto de 4.0 y el cesio (Cs) tiene el valor más bajo de 0.7.
¿Cómo afecta la electronegatividad a los enlaces químicos?
La electronegatividad afecta la polaridad de los enlaces químicos. Si los átomos que forman el enlace tienen una diferencia de electronegatividad alta, entonces el enlace será polar, lo que significa que los electrones se distribuyen de manera desigual entre los átomos. Si la diferencia de electronegatividad es muy alta, entonces el enlace puede ser iónico, lo que significa que uno de los átomos cede completamente sus electrones a otro átomo con una electronegatividad más alta.
¿Qué otros factores influyen en la electronegatividad de los elementos?
Además de la afinidad electrónica, otros factores que influyen en la electronegatividad de los elementos incluyen el tamaño del átomo y la carga nuclear efectiva. En general, los átomos más pequeños y con una carga nuclear efectiva alta tienden a ser más electronegativos que los átomos grandes y con una carga nuclear efectiva baja.
Conclusión y despedida
Conocer los elementos más electronegativos de la tabla periódica es fundamental para entender la polaridad de los enlaces químicos y las reacciones químicas. El flúor, el oxígeno, el cloro, el nitrógeno, el azufre y el carbono son los elementos más electronegativos, y su electronegatividad se mide utilizando el método de Pauling. Además de la afinidad electrónica, otros factores que influyen en la electronegatividad de los elementos incluyen el tamaño del átomo y la carga nuclear efectiva.

Deja una respuesta